Pesquisadores da Austrália desenvolveram um novo andaime biocerâmico 3D capaz de combater bactérias sem depender de antibióticos
Pesquisadores do Laboratório de Nanoengenharia Biomédica da Universidade Flinders, na Austrália, identificaram uma combinação de metal líquido que pode ser a arma secreta na luta global contra a resistência antimicrobiana, prolongando o desempenho de materiais usados em implantes ortopédicos.
Além de combater infecções, a novidade se mostrou mais biocompatível com os ossos, dando aos pacientes potencial para uma cura mais rápida e maior longevidade do dispositivo após grandes cirurgias ortopédicas.
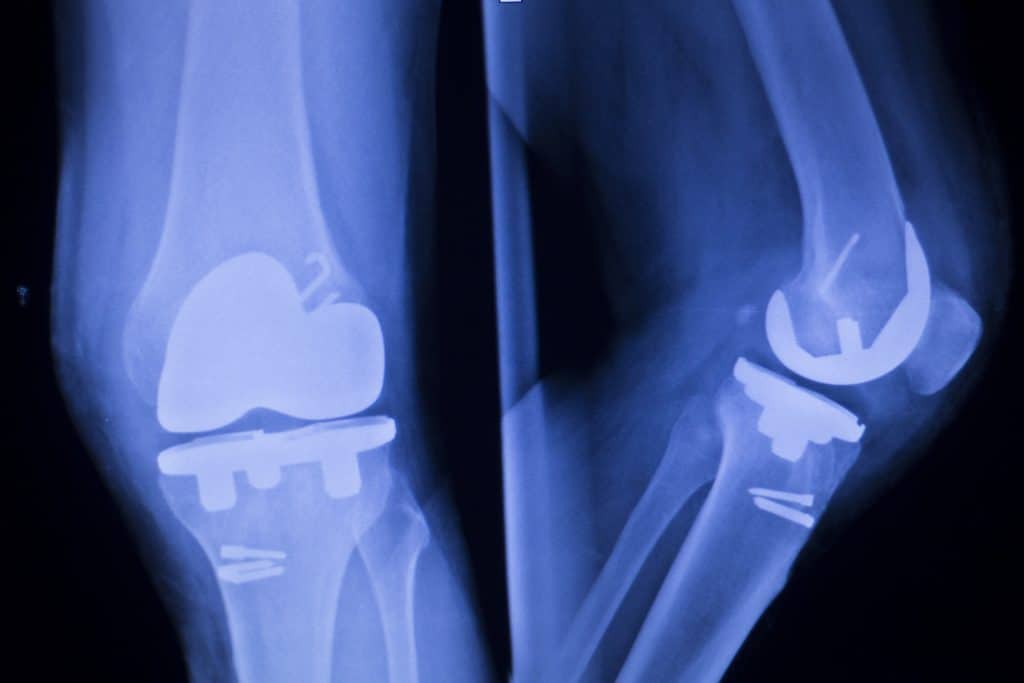
Uma descoberta particularmente útil em um país onde são feitas mais de 85.000 substituições de quadril e joelho anualmente – seja pelo envelhecimento da população, lesões esportivas ou efeitos da obesidade.
“Este novo andaime biocerâmico 3D incorporado com nanopartículas de metal líquido de prata-gálio (Ag-Ga) oferece um biomaterial de dupla função que simultaneamente combate infecções persistentes e promove a regeneração óssea”, afirma o professor associado da Universidade Flinders, Vi-Khanh Truong, autor principal do estudo.
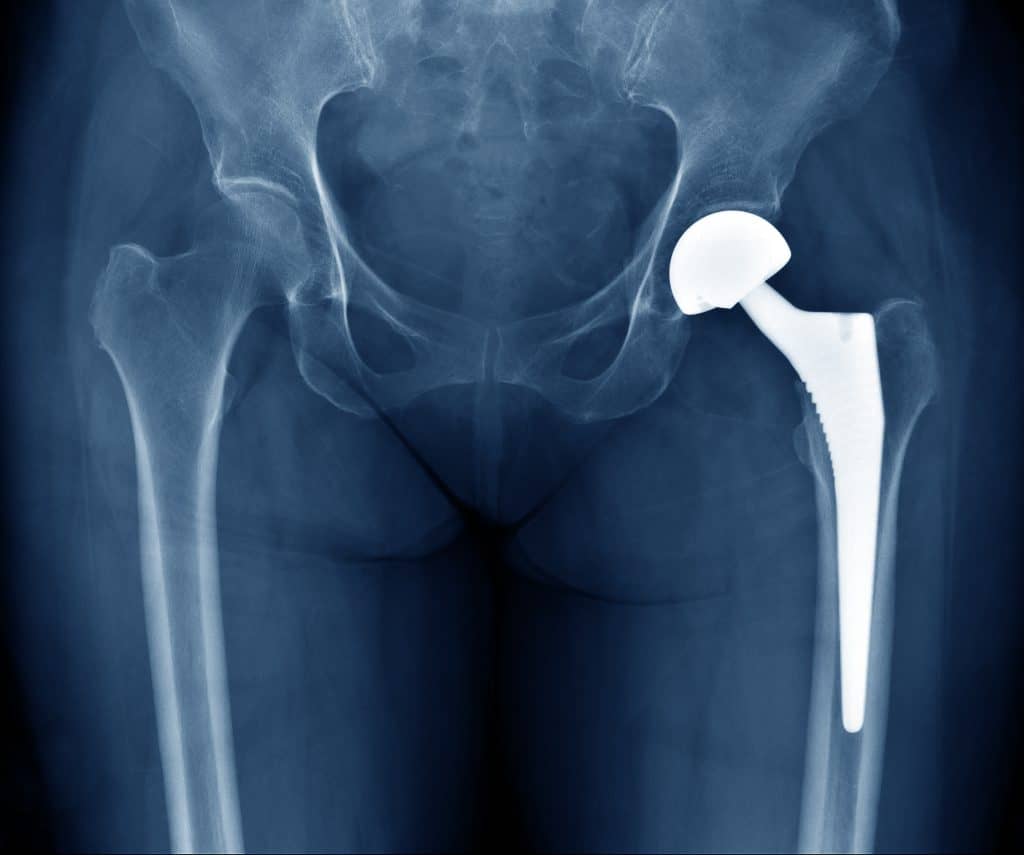
Um problema global
Infecções associadas a implantes continuam sendo um desafio crítico em cirurgia e ortopedia, já que antibióticos sistêmicos estão cada vez mais ineficazes devido à resistência, e cimentos com antibióticos costumam ter vida curta e espectro de ação estreito, afirmam os pesquisadores.
O estudo publicado na revista científica Advanced Functional Materials traz o primeiro caso relatado de integração de nanomateriais à base de metal líquido em uma estrutura cerâmica bioativa de suporte de carga. O arcabouço biocerâmico à base de metal líquido foi integrado com nanopartículas de Ag-Ga em hidroxiapatita.
Nossa abordagem difere fundamentalmente dos materiais convencionais carregados com antibióticos. Em vez de liberação rápida, a estrutura oferece proteção antimicrobiana localizada e sustentada ao mesmo tempo em que auxilia ativamente na cicatrização óssea.
Dr. Ngoc Huu Nguyen, pesquisador de pós-doutorado do projeto.
Os efeitos antibacterianos multidirecionais demonstraram ser eficazes contra uma série de patógenos clinicamente significativos, incluindo Staphylococcus aureus, S. aureus resistente à meticilina (MRSA), Pseudomonas aeruginosa e variantes de pequenas colônias – “que são notoriamente difíceis de eliminar usando antibióticos convencionais”.
Leia Mais:
- ‘Pistola de cola quente’ para ossos pode revolucionar a ortopedia
- É possível quebrar todos os ossos de uma só vez?
- Estudo revela como antibióticos rompem defesa das bactérias
Possíveis aplicações futuras
- Preenchimentos ósseos antimicrobianos para fraturas infectadas, fusões espinhais e cirurgias de revisão;
- Cimentos ósseos de última geração, livres de antibióticos e com ação antimicrobiana mediada por íons;
- Andaimes impressos em 3D específicos para pacientes para defeitos de ressecção craniofacial, de ossos longos e de tumores;
- Dispositivos implantáveis autônomos para ambientes propensos a infecções, como pé diabético e perda óssea relacionada à oncologia.
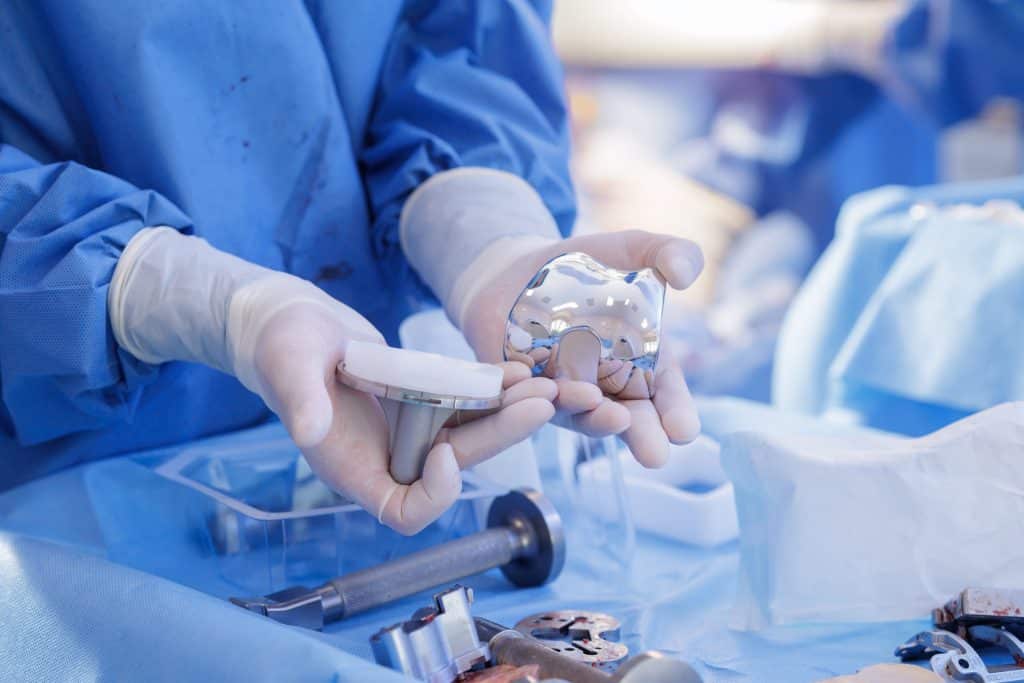
“Essa inovação ajuda a criar uma nova geração de materiais de reparo ósseo que podem prevenir infecções sem depender de antibióticos ao mesmo tempo em que melhoram a integração e a cicatrização dos tecidos”, afirma o professor de Nanoengenharia Biomédica Krasimir Vasilev.

Colaboração para o Olhar Digital
Bruna Barone é formada em Jornalismo pela Faculdade Cásper Líbero. Atuou como editora, repórter e apresentadora na Rádio BandNews FM por 10 anos. Atualmente, é colaboradora no Olhar Digital.




